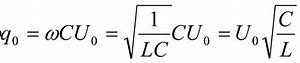Vụ Thuốc Phiện
Người bệnh có nhu cầu tư vấn về thuốc khi khám chữa bệnh tại Bệnh viện Bình Dân, Quý khách vui lòng liên hệ Tổng đài Chăm sóc khách hàng 1900 7123 để được kết nối.
Người bệnh có nhu cầu tư vấn về thuốc khi khám chữa bệnh tại Bệnh viện Bình Dân, Quý khách vui lòng liên hệ Tổng đài Chăm sóc khách hàng 1900 7123 để được kết nối.
MEDGATE – ĐƠN VỊ CUNG CẤP DỊCH VỤ ĐĂNG KÝ LƯU HÀNH THUỐC TẠI VIỆT NAM
Trong bối cảnh ngành dược phẩm ngày càng phát triển, việc đảm bảo an toàn và chất lượng cho các sản phẩm thuốc trở nên quan trọng hơn bao giờ hết. MEDGATE là một đơn vị hàng đầu cung cấp dịch vụ đăng ký lưu hành thuốc tại Việt Nam đối với cả thuốc trong nước và thuốc nước ngoài. MEDGATE cam kết là đối tác tin cậy đồng hành cùng các doanh nghiệp trong ngành dược, hỗ trợ đắc lực trong quá trình đưa sản phẩm ra thị trường.
Dịch vụ đăng ký lưu hành thuốc Medgate
Cơ sở/ đơn vị đứng tên lưu hành thuốc phải đáp ứng các điều kiện sau:
a) Cơ sở/ doanh nghiệp có hoạt động sản xuất, bán buôn, xuất khẩu, nhập khẩu thuốc, nguyên liệu làm thuốc tại Việt Nam;
b) Cơ sở/doanh nghiệp kinh doanh thuốc, nguyên liệu làm thuốc của nước ngoài có văn phòng đại diện tại Việt Nam.
Hồ sơ đề nghị cấp giấy đăng ký lưu hành thuốc dược liệu
b) Giấy ủy quyền đứng tên cơ sở đăng ký (nếu có);
c) Giấy ủy quyền ký tên trên hồ sơ đăng ký (nếu có);
d) Mẫu nhãn thuốc và tờ hướng dẫn sử dụng thuốc dự kiến lưu hành;
đ) Giấy chứng nhận đủ điều kiện kinh doanh dược đối với cơ sở đăng ký của Việt Nam;
e) Giấy tờ pháp lý, giấy phép thành lập văn phòng đại diện tại Việt Nam đối với cơ sở đăng ký nước ngoài;
g) Giấy tờ pháp lý của cơ sở sản xuất dược chất, tá dược, vỏ nang, bán thành phẩm dược liệu, dược liệu;
h) Giấy chứng nhận của cơ sở kiểm nghiệm đối với trường hợp quy định tại khoản 16 Điều 22 Thông tư này;
i) Mẫu nhãn thuốc và tờ hướng dẫn sử dụng thuốc lưu hành thực tế tại nước sản xuất hoặc nước cấp CPP đối với hồ sơ đăng ký thuốc nước ngoài;
k) Giấy chứng nhận CPP đối với hồ sơ đăng ký thuốc nước ngoài;
l) Tài liệu đánh giá việc đáp ứng GMP đối với các trường hợp quy định tại Điều 95 Nghị định số 54/2017/NĐ-CP đối với cơ sở sản xuất thuốc, nguyên liệu làm thuốc nước ngoài khi đăng ký lưu hành tại Việt Nam đối với hồ sơ đăng ký thuốc nước ngoài (trừ trường hợp cơ sở đã được công bố thông tin đáp ứng GMP trên trang thông tin điện tử của Cục Quản lý Dược hoặc cơ sở đã nộp hồ sơ đề nghị Cục Quản lý Dược đánh giá đáp ứng GMP).
m) Giấy chứng nhận nguyên liệu làm thuốc được phép sản xuất hoặc lưu hành ở nước sản xuất đối với hồ sơ đăng ký nguyên liệu làm thuốc sản xuất tại nước ngoài.
*Hồ sơ chất lượng, tiền lâm sàng, lâm sàng theo hướng dẫn ACTD
Hồ sơ đề nghị cấp giấy đăng ký lưu hành thuốc (thuốc hóa dược mới, vắc xin, sinh phẩm)
b) Giấy ủy quyền đứng tên cơ sở đăng ký (nếu có);
c) Giấy ủy quyền ký tên trên hồ sơ đăng ký (nếu có);
d) Mẫu nhãn thuốc và tờ hướng dẫn sử dụng thuốc dự kiến lưu hành;
đ) Giấy chứng nhận đủ điều kiện kinh doanh dược đối với cơ sở đăng ký của Việt Nam;
e) Giấy tờ pháp lý, giấy phép thành lập văn phòng đại diện tại Việt Nam đối với cơ sở đăng ký nước ngoài;
g) Tóm tắt đặc tính sản phẩm đối với thuốc hoá dược mới, vắc xin, sinh phẩm theo Mẫu 6/TT ban hành kèm theo Thông tư này;
h) Giấy tờ pháp lý của cơ sở sản xuất dược chất, tá dược, vỏ nang, bán thành phẩm dược liệu, dược liệu;
i) Giấy chứng nhận của cơ sở kiểm nghiệm đối với trường hợp quy định tại khoản 16 Điều 22 Thông tư này;
k) Kế hoạch quản lý nguy cơ (đối với vắc xin) theo Mẫu 7/TT ban hành kèm theo Thông tư này;
l) Mẫu nhãn thuốc và tờ hướng dẫn sử dụng thuốc lưu hành thực tế tại nước sản xuất hoặc nước cấp CPP đối với hồ sơ đăng ký thuốc nước ngoài;
m) Giấy chứng nhận CPP đối với hồ sơ đăng ký thuốc nước ngoài;
n) Tài liệu đánh giá việc đáp ứng GMP đối với các trường hợp quy định tại Điều 95 Nghị định số 54/2017/NĐ-CP đối với cơ sở sản xuất thuốc, nguyên liệu làm thuốc nước ngoài khi đăng ký lưu hành tại Việt Nam đối với hồ sơ đăng ký thuốc nước ngoài (trừ trường hợp cơ sở đã được công bố thông tin đáp ứng GMP trên trang thông tin điện tử của Cục Quản lý Dược hoặc cơ sở đã nộp hồ sơ đề nghị Cục Quản lý Dược đánh giá đáp ứng GMP).
*Hồ sơ chất lượng, tiền lâm sàng, lâm sàng theo hướng dẫn ACTD
Căn cứ pháp lý về đăng ký lưu hành thuốc
– Thông tư 08/2022/TT-BYT là thông tư quy định việc ĐK lưu hành thuốc, nguyên liệu làm thuốc.
– Thông tư 07/2017/TT-BYT là thông tư ban hành DM thuốc không kê đơn
– Thông tư 06/2017/TT-BYT là thông tư ban hành DM thuốc độc và nguyên liệu độc làm thuốc
– Thông tư 42/2017/TT-BYT là thông tư ban hành DM dược liệu độc làm thuốc
– Thông tư 21/2018/TT-BYT là thông tư quy định việc đăng ký lưu hành thuốc cổ truyền, dược liệu
– Thông tư 20/2017/TT-BYT là thông tư quy định về thuốc và nguyên liệu làm thuốc phải kiểm soát đặc biệt
– Thông tư 01/2018/TT-BYT là thông tư quy định ghi nhãn thuốc, nguyên liệu làm thuốc và tờ hướng dẫn sử dụng
Giới thiệu dịch vụ đăng ký lưu hành thuốc
Dịch vụ đăng ký lưu hành thuốc là quá trình mà các doanh nghiệp phải tiến hành để có thể lưu hành và bán các sản phẩm thuốc trên thị trường.
Quá trình đăng ký lưu hành thuốc là công việc mất nhiều thời gian, đồng thời đòi hỏi chuyên viên đăng ký phải có kiến thức chuyên sâu, hiểu biết vững chắc về quy trình, và có kinh nghiệm trong làm hồ sơ, luôn liên tục theo dõi và cập nhật về các quy định, yêu cầu mới từ cơ quan quản lý. Điều này giúp họ áp dụng những thông tin mới nhất vào quá trình làm việc, đảm bảo tính hiệu quả và tuân thủ đầy đủ các quy định.
Thời hạn hiệu lực của số đăng ký lưu hành thuốc
(Theo điều 8, Thông tư 08/2022/TT-BYT: Quy định việc đăng kí lưu hành thuốc, nguyên liệu làm thuốc)
1. Thời hạn hiệu lực của giấy đăng ký lưu hành thuốc là 05 (năm) năm kể từ ngày cấp hoặc gia hạn.
2. Thời hạn hiệu lực của giấy đăng ký lưu hành là 03 (ba) năm kể từ ngày cấp đối với các thuốc sau:
a) Thuốc mới, vắc xin lần đầu cấp giấy đăng ký lưu hành, sinh phẩm tham chiếu, sinh phẩm tương tự lần đầu cấp giấy đăng ký lưu hành tại Việt Nam;
b) Thuốc cùng dược chất, nồng độ, hàm lượng, dạng bào chế với thuốc mới mà thuốc mới đó chưa được cấp giấy đăng ký lưu hành với thời hạn 05 (năm) năm;
c) Các trường hợp tiếp tục theo dõi an toàn, hiệu quả theo ý kiến tư vấn của Hội đồng;
d) Thuốc thuộc trường hợp quy định tại điểm a, b và c khoản này nhưng tại thời điểm nộp hồ sơ gia hạn giấy đăng ký lưu hành mà chưa có báo cáo an toàn, hiệu quả vì lý do chưa lưu hành hoặc có báo cáo an toàn, hiệu quả nhưng số lượng thuốc sử dụng, số lượng bệnh nhân, thời gian sử dụng còn hạn chế theo ý kiến của Hội đồng hoặc có khuyến nghị của cơ sở khám chữa bệnh về việc cần tiếp tục theo dõi an toàn, hiệu quả.
3. Thời hạn nộp hồ sơ đăng ký gia hạn: Trong vòng 12 tháng trước khi giấy đăng ký lưu hành hết hiệu lực, cơ sở đăng ký phải tiến hành nộp hồ sơ gia hạn giấy đăng ký lưu hành, tránh việc gián đoạn thời gian phân phối thuốc trên thị trường.
Liên hệ ngay với MEDGATE để được tư vấn miễn phí qua hotline 098.546.1894 hoặc email [email protected]
Yêu cầu của thuốc được cấp giấy đăng ký lưu hành tại Việt Nam:
a) Bảo đảm về tính an toàn, hiệu quả;
b) Được sản xuất tại cơ sở sản xuất thuốc đáp ứng điều kiện theo quy định
c) Được sản xuất theo quy trình sản xuất thuốc và đạt tiêu chuẩn chất lượng theo quy định
** Đối với thuốc chưa có giấy đăng ký lưu hành, cơ sở tiến hành đăng ký thuốc khi nộp hồ sơ đề nghị cấp giấy đăng ký lưu hành thuốc nước ngoài phải nộp hồ sơ đề nghị đánh giá cơ sở sản xuất đáp ứng thực hành tốt sản xuất trong các trường hợp sau:
a) Cơ sở sản xuất nước ngoài lần đầu có thuốc đăng ký lưu hành tại Việt Nam;
b) Thuốc được sản xuất trên dây chuyền chưa được Bộ Y tế đánh giá;
c) Nguyên liệu làm thuốc là dược chất lần đầu được đăng ký lưu hành tại Việt Nam;
d) Cơ sở sản xuất nước ngoài lần đầu có dược liệu đăng ký lưu hành tại Việt Nam.
** Đối với thuốc đã có giấy đăng ký lưu hành nhưng cơ sở sản xuất thuốc, nguyên liệu làm thuốc chưa được Bộ Y tế đánh giá, cơ sở tiến hành đăng ký thuốc nộp hồ sơ đề nghị đánh giá cơ sở sản xuất đáp ứng thực hành tốt sản xuất trong các trường hợp sau:
a) Khi nộp hồ sơ đề nghị gia hạn giấy đăng ký lưu hành thuốc
b) Khi nộp hồ sơ đề nghị cấp giấy đăng ký lưu hành thuốc do thay đổi địa điểm của cơ sở sản xuất theo quy định tại điểm b hoặc c khoản 2 Điều 55 của Luật dược.
** Trường hợp thuốc được sản xuất theo nhiều công đoạn sản xuất tại nhiều cơ sở sản xuất khác nhau, cơ sở đăng ký phải nộp hồ sơ đề nghị đánh giá đối với tất cả các cơ sở sản xuất tham gia vào sản xuất thuốc.